Estas células afectadas se encuentran en una región llamada “sustancia negra” y tienen una función clave: producir dopamina, una molécula esencial para controlar el movimiento. Cuando estas neuronas desaparecen surgen los síntomas más conocidos como temblores, rigidez muscular, lentitud y dificultades para caminar.
Durante décadas, los tratamientos se han basado en compensar la pérdida de dopamina en el cerebro. Si bien es cierto que fármacos como la levodopa pueden mejorar notablemente los síntomas, presentan una limitación: no detienen la enfermedad ni recuperan las neuronas perdidas.
En otras palabras, se actúa sobre las consecuencias del problema (la pérdida de dopamina), pero no se arregla su origen (la muerte de neuronas). Una nueva estrategia está empezando a cambiar ese enfoque. En lugar de limitarse a compensar el daño, intenta repararlo.
¿Y si pudiésemos reemplazar las neuronas?
La terapia celular parte de un concepto sorprendentemente sencillo. Si el párkinson destruye las neuronas que producen la dopamina, ¿por qué no reemplazarlas por otras nuevas?
Durante años esta idea fue más un sueño que una posibilidad real. Las neuronas son extremadamente complejas. No basta con introducir cualquier célula en el cerebro: deben ser del tipo correcto, sobrevivir al trasplante, integrarse en los circuitos neuronales y producir dopamina de manera controlada.
El gran salto llegó con el desarrollo de las células madre pluripotentes inducidas (iPSC). Estas fueron descritas por el grupo de investigación liderado por el científico japonés Shinya Yamanaka, que recibió por ello el Premio Nobel de Fisiología o Medicina en 2012.
Las iPSC se obtienen reprogramando células adultas, como las de la piel, para devolverlas a un estado similar al embrionario. Desde ahí pueden convertirse en muchos tipos celulares, incluidas las neuronas productoras de dopamina.
Gracias a esta tecnología, la idea de reemplazar neuronas dejó de ser ciencia ficción.
Dos ensayos clínicos que marcan un antes y un después
En 2025 se publicaron en la revista Nature dos ensayos clínicos pioneros que han llevado esta estrategia al cerebro humano.
En uno de ellos los investigadores trasplantaron neuronas productoras de dopamina derivadas de células madre pluripotentes inducidas a pacientes con párkinson. El estudio mostró que el procedimiento era seguro y que las células implantadas podían sobrevivir durante largos periodos de tiempo y producir dopamina en el cerebro humano.
El segundo ensayo utilizó neuronas derivadas de células embrionarias humanas (hES). De nuevo, los resultados indicaron una buena tolerabilidad y mostraron señales de beneficio clínico duradero.
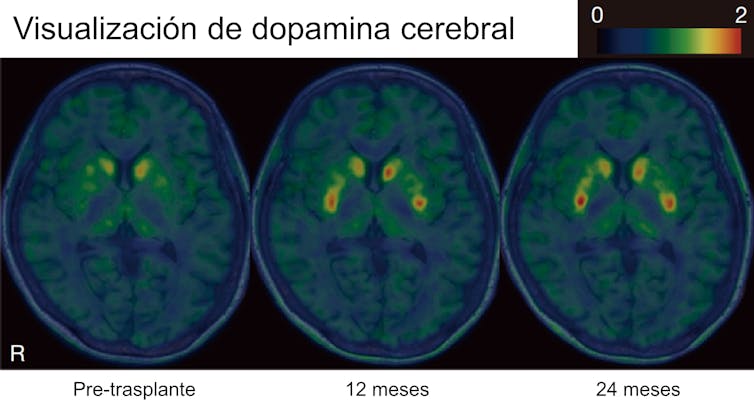 Comprobación de la producción de dopamina por parte de las neuronas trasplantadas en un paciente a los 12 y 24 meses tras la operación. Imagen traducida del estudio https://www.nature.com/articles/s41586-025-08700-0. CC BY-NC-ND
Comprobación de la producción de dopamina por parte de las neuronas trasplantadas en un paciente a los 12 y 24 meses tras la operación. Imagen traducida del estudio https://www.nature.com/articles/s41586-025-08700-0. CC BY-NC-ND
¿Qué se ha observado en los pacientes?
Aunque todavía es pronto para sacar conclusiones definitivas, los estudios han mostrado varios resultados prometedores:
-
Las células trasplantadas sobreviven en el cerebro.
-
Producen dopamina de forma detectable.
-
Algunos pacientes presentan mejoría en sus síntomas motores.
-
No se han observado problemas graves de seguridad a corto plazo.
Esto no significa que la terapia esté lista para uso clínico general, pero sí que el enfoque es biológicamente viable.
¿Por qué este avance es tan importante?
El párkinson es una enfermedad neurodegenerativa progresiva. Con el tiempo la pérdida neuronal continúa y los tratamientos actuales se vuelven menos eficaces. La terapia celular podría ofrecer varias ventajas clave:
-
Actuar sobre la causa del problema, no únicamente sobre sus consecuencias.
-
Restaurar la producción natural de dopamina en lugar de administrarla de manera externa.
-
Proporcionar beneficios duraderos, potencialmente durante años.
Pero aún no es una cura
Es importante mantener expectativas realistas: estos avances no significan que exista ya una cura disponible.
Los ensayos realizados hasta ahora incluyen pocos pacientes, y el seguimiento aún es limitado. Es necesario comprobar que las células trasplantadas sobreviven durante muchos años y que los beneficios se mantienen en el tiempo.
Además, no todos los pacientes con párkinson son iguales. La enfermedad evoluciona de forma distinta en cada persona y todavía no está claro quiénes se beneficiarán más del trasplante.
Por último, el párkinson es una enfermedad compleja que, con el tiempo, afecta a más sistemas además de las neuronas productoras de dopamina. Reemplazar estas células podría mejorar mucho los síntomas motores, pero probablemente no resolverá todos los aspectos de la enfermedad.
Un camino largo, pero prometedor
A pesar de las limitaciones, estos ensayos representan un hito histórico. Por primera vez la comunidad científica dispone de evidencia clínica de que reemplazar neuronas productoras de dopamina en humanos es factible y potencialmente beneficioso.
La terapia celular aún está en sus primeras fases, pero marca una dirección clara. La ruta consiste en avanzar desde tratamientos puramente sintomáticos hacia estrategias capaces de reparar el cerebro.
Para millones de personas que viven con la enfermedad de Parkinson este camino todavía es largo. Pero, por primera vez en décadas, la pregunta ya no es si podremos intentar reconstruir las neuronas perdidas, sino cuándo y en qué pacientes podrá hacerse de forma segura y eficaz.![]()
Tania Payo Serafín, Investigadora predoctoral en Biomedicina y Ciencias de la Salud, Universidad de León; Carolina Méndez Blanco, Profesora de Fisiología (Ciencias Biomédicas), Universidad de León y Jennifer Martínez Geijo, Estudiante predoctoral del programa de Biomedicina y Ciencias de la Salud, Universidad de León
Este artículo fue publicado originalmente en The Conversation. Lea el original.










.gif)